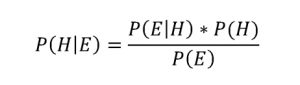Czy należy wątpić w efektywność współczesnej medycyny?

Od oświecenia długość życia w Europie podwoiła się. O wierze w efektywność terapii medycznych świadczy nieustannie rosnący popyt: w krajach wysoko uprzemysłowionych z roku na rok wydatki na opiekę medyczną rosną o kilka procent szybciej niż dochody. W takich okolicznościach systematyczne wątpienie w dorobek medycyny, czyli cel pracy Jacoba Stegengi (2018), wydaje się zakrawać na szaleństwo.
Medycyna wydaje się jedną z nauk stosowanych, które odnoszą największe sukcesy. Kuracje farmakologiczne pozwalają wyleczyć choroby, które kiedyś dziesiątkowały populację. Dla przykładu, odkrycie penicyliny oraz stworzenie syntetycznych antybiotyków pozwala zwalczyć zdecydowaną większość zakażeń bakteryjnych. Od oświecenia długość życia w Europie podwoiła się. O wierze w efektywność terapii medycznych świadczy nieustannie rosnący popyt: w krajach wysoko uprzemysłowionych z roku na rok wydatki na opiekę medyczną rosną o kilka procent szybciej niż dochody. W takich okolicznościach systematyczne wątpienie w dorobek medycyny, czyli cel pracy Jacoba Stegengi (2018), wydaje się zakrawać na szaleństwo. Jego stanowisko – ‘medyczny nihilizm’ – należy rozumieć jako formę radykalnego sceptycyzmu, wątpienia lub braku wiary w efektywność współczesnych terapii medycznych (Ibidem: 2). Krytyka skupia się na opracowanych współcześnie (tj. w ostatnich kilkudziesięciu latach) terapiach farmakologicznych. Stegenga przedstawia argument oparty na wnioskowaniu bayesowskim, zgodnie z którym prawdopodobieństwo efektywności terapii H przy danych dowodach E, tj. P(H|E) jest wprost proporcjonalna do iloczynu prawdopodobieństwa uzyskania dowodów na efektywność terapii, jeżeli byłaby ona efektywna P(E|H) i prawdopodobieństwa jej efektywności a priori P(H) oraz odwrotnie proporcjonalna do prawdopodobieństwa, że otrzymamy pozytywne wyniki pomimo nieefektywności terapii P(E), co wyraża się formalnie jako (Stegenga 2018: 176):
Gdzie:
P(H|E) – prawdopodobieństwo warunkowe hipotezy H (hipoteza, że terapia jest efektywna) przy danych wynikach E potwierdzających jej skuteczność;
P(E|H) – prawdopodobieństwo uzyskania dowodów na efektywność terapii, jeżeli byłaby ona efektywna;
P(H) – prawdopodobieństwo a priori, że terapia jest skuteczna;
P(E) – prawdopodobieństwo, że zaobserwuje się dowody E potwierdzające skuteczność terapii pomimo jej nieefektywności.
Stegenga formułuje główny argument również w ten sposób: niskie prawdopodobieństwo efektywności nowych leków wynika z [1] niskiej efektywności współczesnych kuracji farmakologicznych, co powoduje, że P(E|H) jest niskie, [2] niskiego prawdopodobieństwa a priori, że nowy lek będzie efektywny (niskie P(H)) oraz [3] wysokiego prawdopodobieństwa, że wyniki badań medycznych dokumentujących działanie rozważanego leku nie wynikają z rzeczywistej efektywności terapii (P(E) wysokie).
Początkiem pesymistycznej analizy procesu leczenia jest obrona popularnej wśród lekarzy (np. Cavalli i in. 2009: 470) hybrydowej definicji choroby, zgodnie z którą choroba jest stanem organizmu [a] biologicznie dysfunkcyjnym (np. układ odpornościowy jest osłabiony) oraz [b] szkodliwym (niska odporność prowadzi do rozwoju chorób i śmierci). Akceptacja tej naturalistyczno-normatywnej (hybrydowej) definicji ma ważne implikacje dla rozważań efektywności farmaceutyków. Aby lek mógł być uznany za efektywny, musi on albo oddziaływać na mechanizm przyczynowy choroby, albo poprawiać dobrostan chorego. Idealnymi lekami są substancje, które działają jak „magiczne pociski” (ang. magic bullets), czyli są specyficzne (działają tylko na mechanizm przyczynowy choroby i nie powodują skutków ubocznych) oraz efektywne (czyli zdolne do wyleczenia). Przykładem takiej substancji jest penicylina, która, blokując tworzenie peptydoglikanu, budulca ścian komórkowych bakterii, powoduje ich śmierć (jest efektywna) oraz jest specyficzna, gdyż komórki zwierząt nie posiadają ścian komórkowych (por. Moore 2009: 93). Stegenga (Ibidem: 53) argumentuje, że niewiele leków zbliża się do ideału magicznego pocisku. Po pierwsze, przegląd skutków stosowania współczesnych farmaceutyków wskazuje, że wśród repertuaru dostępnych już leków niewiele jest substancji tak efektywnych jak penicylina lub insulina. Po drugie, ograniczona skuteczność dostępnych leków oraz skomplikowanie mechanizmów chorobowych pozwala przypuszczać, że efektywność opracowanych w przyszłości farmaceutyków będzie niewielka.
Poza trudnościami związanymi z niewielką liczbą „magicznych pocisków”, medycynę trapią problemy medykalizacji i fabrykowania chorób (ang. disease-mongering). Przedmiotem niektórych interwencji farmakologicznych są stany fizjologiczne, które nie są chorobami (nie są dysfunkcyjne) zgodnie z powyższą definicją hybrydową. Niektóre definicje chorób rozszerza się z biegiem czasu, czego dobrym przykładem jest obniżanie poziomu cholesterolu we krwi uważanego za wysoki, tj. wymagający interwencji farmakologicznej (Ibidem: 47). Natomiast inne schorzenia fabrykuje się, czyli opisuje normalne stany fizjologiczne jako choroby oraz aplikuje (zazwyczaj nieefektywne) leki, czego przykładem może być syndrom niespokojnych nóg (Ibidem: 48). Innym przykładem jest zespół nadpobudliwości psychoruchowej z deficytem uwagi (ADHD) leczony metylofenidatem (Ritalin). Efektami terapii jest zmniejszenie aktywności ruchowej i liczby interakcji społecznych w krótkim okresie, co może być uznane za pozytywne efekty przez wychowawców dzieci, lecz długoterminowe badanie nie pozwoliło zaobserwować wpływu terapii na sukcesy w szkole (Stegenga 2018: 135; 172).
Inne schorzenia fabrykuje się, czyli opisuje normalne stany fizjologiczne jako choroby oraz aplikuje (zazwyczaj nieefektywne) leki, czego przykładem może być syndrom niespokojnych nóg. Innym przykładem jest zespół nadpobudliwości psychoruchowej z deficytem uwagi (ADHD) leczony metylofenidatem (Ritalin).
Argument metodologiczny opiera się na pokazaniu, że metody badawcze stosowane w medycynie (od projektowania eksperymentów, poprzez analizę zebranych danych, do metaanalizy literatury empirycznej) są podatne na wpływy (ang. malleable, dosł. kowalne) i umożliwiają manipulację i uzyskanie wyników oczekiwanych przez podmioty przeprowadzające badania. Przykładem metody podatnej na modyfikacje wyników jest metaanaliza, mimo iż uważa się ją za metodę najbardziej wiarygodną i ulokowaną na szczycie hierarchii medycyny opartej na dowodach. Metoda ta bazuje na założeniu, że sumaryczna analiza wyników wielu eksperymentów daje pewniejsze rezultaty ze względu na większą próbę (większą liczbę uczestników badania klinicznego). Jednak, jak argumentuje Stegenga (2018: 84-97), przeprowadzenie metaanalizy wymaga podjęcia wielu decyzji metodologicznych dotyczących oceny jakości analizowanych eksperymentów i metod statystycznych. Dokonane wybory determinują uzyskane wyniki, co sprawia, że nie są one obiektywne. Bardziej zaawansowaną wersją metaanalizy są narzędzia oceny jakości eksperymentów (ang. Quality Assessment Tools, QATs). Podobnie jak metaanaliza, służą one wyciągnięciu wniosków na podstawie analizy wielu eksperymentów badających wpływ tej samej substancji, jednak są bardziej zaawansowane i opierają się na przypisaniu wag do wyników poszczególnych eksperymentów określających ich jakość. Działanie takie ma na celu, by (przynajmniej w założeniu) badania kliniczne niskiej jakości nie wpływały na ostateczną konkluzję. Stegenga omawia wyniki badań porównujących rezultaty zastosowania odmiennych narzędzi QAT lub analiz przeprowadzonych przez różne zespoły, pokazując, że metaanaliza nie zapewnia porównywalnych wyników uzyskanych za pomocą różnych narzędzi lub przeprowadzanych przez innych statystyków (Ibidem: 104-106).
Nie wydaje się, by podatność na wpływy i brak obiektywizmu metod badawczych stosowanych w medycynie były argumentem przekonującym. Od czasu francuskiego konwencjonalizmu jesteśmy świadomi, że teorie są konwencjami i nie mają charakteru obiektywnego. Na gruncie filozofii medycyny już Ludwik Fleck argumentował, że wyniki naszych badań i przedmioty postrzegania zależne są od naszych założeń i przesądów. Również inne nauki empiryczne, których przykładem może być ekonometria, nie są obiektywne w tym sensie: wybór narzędzi statystycznych determinuje otrzymane wyniki (Maziarz 2017). Sam brak obiektywizmu nie powinien być argumentem na rzecz nihilizmu. Brak obiektywizmu metod statystycznych nie przemawia za odrzuceniem wszystkich wyników, lecz jest raczej przyczynkiem do rozważań jak, pomimo podatności badań na wpływy, uzyskiwać użyteczne wyniki. Jednak Stegenga w kolejnych rozdziałach pokazuje, w czym tkwi prawdziwy problem. Mianowicie, koncerny farmaceutyczne wykorzystują podatność metod badawczych na manipulacje, by uzyskać oczekiwane (z góry założone) wyniki. Przykładem takich działań jest nieupublicznianie wyników badań pierwszej fazy klinicznej (mających na celu ustalenie dawkowania), gdy odkrywa się silną toksyczność nowych farmaceutyków (Ibidem: 134-152). Podobnie, zależności finansowe motywują badaczy do wykorzystania podatności metod badawczych na manipulacje, by osiągnąć z góry założone wyniki (154-162).
Jeżeli prawdopodobieństwo, że nowo opracowywany lek okaże się magicznym pociskiem jest niewielkie, a koncernom farmaceutycznym, które wydały duże środki na opracowanie i wstępne testy nowego farmaceutyku, zależy na pokazaniu jego efektywności i niskiej szkodliwości, to mają one motywację finansową, by przedstawić dowody, że sprzedawane farmaceutyki są bardziej efektywne i powodują mniej skutków ubocznych niż w istocie. „Naginanie” wyników badań jest możliwe ze względu na omówioną powyżej cechę metod badawczych stosowanych w medycynie. Stegenga (2018: 169-171) przytacza szereg leków, które zostały wycofane z użycia, ponieważ po wprowadzeniu ich do obrotu i wykorzystania poza otoczeniem eksperymentalnym okazało się, że przynoszą one więcej szkody niż pożytku. Najczęściej stosowanym lekiem, który wycofano ze względu na skutki uboczne był rofekoksyb (Vioxx), zaakceptowany przez Food and Drag Administration (FDA) w roku 1999 do leczenia reumatoidalnego zapalenia stawów (RZS) i kilku innych chorób. Przepisujący go lekarze zauważyli, że pacjenci leczeni rofekoksybem często przechodzili zawały i udary. Szacuje się, że poszkodowanych zostało od 90 do 140 tysięcy pacjentów (Ibidem: 171). Wyniki eksperymentu VIGOR pokazały, że rofekoksyb zwiększa czterokrotnie ryzyko wystąpienia poważnych zaburzeń układu krążenia w stosunku do innych leków na RZS, jednak nie skłoniły one producenta do wycofania Vioxxu z rynku (Karha i Topol 2004); nastąpiło to dopiero kilka lat później.
Poza kwestią wykrywania skutków ubocznych, z badaniami klinicznymi wiąże się też inny problem. Mianowicie, są one projektowane w ten sposób, by wykryć nawet marginalną efektywność testowanego leku. Przykładem może być testowanie leków na depresję z grupy inhibitorów zwrotnego wychwytu serotoniny (SSRI) takich jak fluoksetyna, której popularność została opowiedziana na srebrnym ekranie przez film Pokolenie P z 2001 roku wyreżyserowany na podstawie książki Elizabeth Wurtzel . Aby określić zaawansowanie depresji, stosuje się m.in. skalę HAM-D, opartą na szeregu pytań ankietowych: im mniejszy wynik, tym mniejszy stopień zaawansowania choroby (zdrowszy pacjent). Jak zauważa Stegenga (2018: 115-119), niektóre pytania są tendencyjne, a sam udział w badaniu może zmienić udzielane odpowiedzi. Dla przykładu, zaprzeczenie, że jest się chorym na depresję oznacza przyznanie 2 punktów. Akceptacja złego samopoczucia, ale wskazanie innych czynników jako przyczyn (np. pogody, przepracowania itd.) oznacza przyznanie 1 punktu. Przyznanie się do cierpienia na depresję to 0 punktów. Biorąc pod uwagę, że leki antydepresyjne z grupy SSRI średnio poprawiają wynik o 1,8 punktu (Ibidem: 131), wystarczy, że udział w badaniu uświadomi pacjentowi, że jest chory, by odnotować poprawę wyników większą niż średnia efektywność leków antydepresyjnych. Stegenga przedstawia leki antydepresyjne jako przykład terapii charakteryzującej się marginalnym efektem klinicznym.
Koncerny farmaceutyczne wykorzystują podatność metod badawczych na manipulacje, by uzyskać oczekiwane (z góry założone) wyniki. Przykładem takich działań jest nieupublicznianie wyników badań pierwszej fazy klinicznej (mających na celu ustalenie dawkowania), gdy odkrywa się silną toksyczność nowych farmaceutyków.
Czy medyczny nihilizm rozumiany jako systematyczny sceptycyzm względem współcześnie wprowadzanych leków jest stanowiskiem możliwym do utrzymania? Jak przyznaje sam Stegenga (2018: 5), gdyby padł ofiarą poważnego wypadku, miejscem, w którym chciałby przebywać, byłby oddział intensywnej terapii. Autor przyznał to, mimo że do sedacji (uspokojenia) podczas przeprowadzanych tam zabiegów lekarze wykorzystaliby deksmedetomidynę, wprowadzoną na rynek w 1999 roku (Blaine et al. 2007). Przedmiotem nihilistycznego stanowiska bronionego w książce są współczesne (tj. wprowadzone w ostatnich dekadach) terapie farmakologiczne, więc Stegenga wątpi również w efektywność niektórych leków podawanych na oddziałach intensywnej terapii. Jednak, pomimo nihilizmu, chciałby być leczony. Dlatego należy podkreślić, że autor nie zachęca do przyjęcia stanowiska antynaukowego, nie podważa wszystkich osiągnięć medycyny, ani tym bardziej nie zachęca do stosowania terapii medycyny alternatywnej. Jak sam wskazuje (Ibidem: 182), jego argumenty jeszcze silniej sprzeciwiają się terapiom opartym na pseudo-naukowych teoriach. Książka jest głosem nakłaniającym do analizy najlepszych dostępnych danych i wyników badań w odpowiedni sposób. Niektóre leki są magicznymi pociskami i powinniśmy je stosować. Jednak sceptycyzm i analiza przypadku każdego farmaceutyku biorąca pod uwagę ograniczenia i stronniczość wyników badań medycznych powinny prowadzić do ograniczenia liczby interwencji, na które się decydujemy.
Literatura
Karha, J., & Topol, E.J. (2004), The sad story of Vioxx, and what we should learn from it, ”Cleveland Clinic Journal of Medicine” 71 (12): 933-939.
Maziarz, M. (2017), The Reinhart-Rogoff controversy as an instance of the ‘emerging contrary result’ phenomenon, „Journal of Economic Methodology” 24 (3): 213-225.
Moore, P. (2009), Tajemnicze choroby współczesnego świata. Bellona, Warszawa.
Stegenga, J. (2018), Medical nihilism. Oxford University Press, Oxford.
Mariusz Maziarz – doktorant na Uniwersytecie Ekonomicznym we Wrocławiu
Artykuł powstał dzięki dofinansowaniu z Instytutu Filozofii UJ w ramach projektu „Zintegrowany system zdalnego nauczania w IF UJ”.